
香港大學理學院化學系葉志成范港喜基金教授(生物無機化學)孫紅哲及李嘉誠醫學院微生物學系助理教授袁碩峰率領研究團隊發現基於膠體枸櫞酸鉍和乙酰半胱氨酸的組合藥物CBS+3NAC實現通過口服給藥的方式顯著抑制在動物感染模型中的新冠病毒複製和繁殖,研究目前已於國際學術期刊《化學科學》發表並已申請美國專利。
據了解孫紅哲團隊此前已篩選一系列金屬藥物和相關化合物,發現含有金屬鉍的藥物在細胞水平和動物模型中能顯著降低新冠病毒載量,此研究已於前年在《自然 微生物》發表。
港大表示膠體枸櫞酸鉍和水楊酸鉍易於胃酸條件下水解而沉澱,故其抗病毒活性難以通過口服方式發揮作用,而「雞尾酒療法」中的組分乙酰半胱氨酸可與強親硫性鉍離子結合形成高水溶性活性組分,在人工膜、Caco-2 細胞體外吸收模型和大鼠腸管外翻模型中,乙酰半胱氨酸的聯合使用能顯著提升鉍離子穿膜性,並可通過與黏蛋白的硫交換的過程促進鉍離子在胃腸道細胞進一步吸收;藥代動力學研究顯示大鼠在口服CBS+3NAC後所測得的血鉍濃度及肺部有效鉍含量均顯著增加。
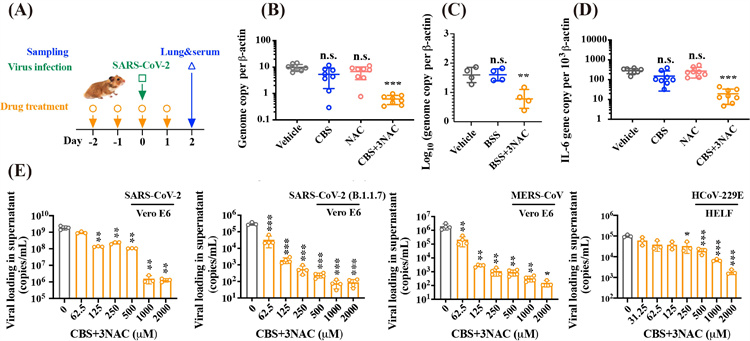
CBS 和 NAC 在體外和體內均表現出廣譜抗冠狀病毒效⼒。 (A)通過⼜服給藥在第 -2、-1、0 和 1 天給予對照溶劑、CBS (300 mg/kg)、BSS (300 mg/kg)、NAC (370 mg/kg)、CBS (300 mg/kg)+3NAC (370 mg) 進⾏治療的⽅案 /kg) 或 BSS (300 mg/kg)+3NAC (405 mg/kg)。倉鼠在第 0 天受到病毒攻擊。在第 2 天收集組織樣本。 (B) 分別接受對照溶劑、CBS、NAC 和 CBS+3NAC 治療的倉鼠肺組織中的病毒產量。 (C) 分別接受對照溶劑、CBS、NAC 和 CBS+3NAC 治療的倉鼠肺組織中細胞因⼦ IL-6 基因的表達⽔平。(E) CBS+3NAC 以濃度依賴的⽅式抑製⼈類致病性冠狀病毒在⼈類細胞模型中的複製,分別顯⽰為 Vero E6 細胞中的 SARS-CoV-2︔ 在 Vero E6 細胞中的 SARS-CoV-2 (B .1.1.7 變體); 在 Vero E6 細胞中的 MERS-CoV 和在 HELF 細胞中的 HCoV-229E。
此外,港大研究團隊於敘利亞金色倉鼠的感染模型中證明,經口服給藥的鉍劑膠體枸櫞酸鉍及BSS在與乙酰半胱氨酸的雞尾酒聯合療法中能展現強大抗病毒活性。藥物組合CBS+3NAC大幅降低新冠病毒載量10倍以上並顯著緩解動物肺部與感染相關病徵。所給藥物劑量僅出現可逆轉的輕微腎毒性且並未顯示出有明顯系統性毒性,在細胞水平上,CBS+3NAC雞尾酒療法對新冠病毒及其變異株B1.1.7、中東呼吸綜合症病毒和人類冠狀病毒等的廣譜的抗病毒效力。
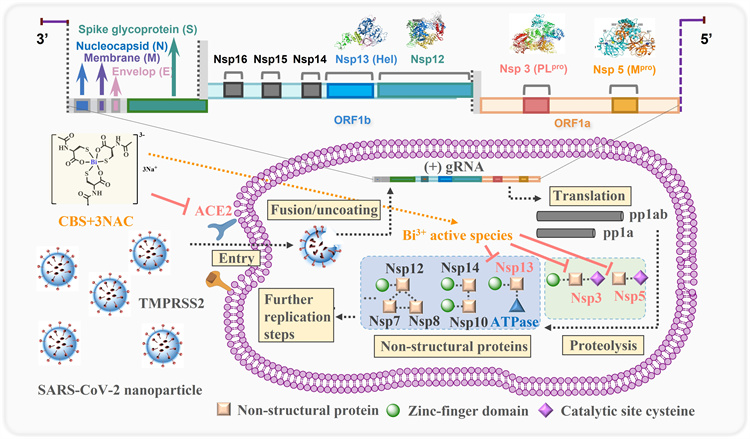
含鉍藥物與⼄酰半胱氨酸藥物雞尾酒療法作⽤機理。含鉍藥物對各種 CoV 的泛抑製活性可能源於它們在病毒複製周期中靶向多種病毒酶的能⼒。可以有效地靶向病原體中蛋⽩質的 Zn2+-半胱氨酸位點,例如,可以通過靶向活性位點(PLpro 和 Mpro)中的關鍵半胱氨酸殘基或結構鋅指結構域(PLpro 和 Hel)來滅活病毒半胱氨酸蛋⽩酶,甚至靶向⼈體細胞中與病毒進入密切相關的其他含鋅 ⾦屬蛋⽩ (ACE2)。
港大研究團隊在後續研究上還發現CBS+3NAC可能對病毒複製周期中的多個生物合成等過程產生影響。CBS+3NAC能有效抑製新型冠狀病毒受體ACE2、病毒解旋酶、主蛋白酶、木瓜蛋白酶等與新冠病毒感染相關的重要蛋白酶的活性,呈現典型多靶點藥物特性,故能取得廣譜而高效抑製冠狀病毒複製效果。
頂圖:葉志成×范港喜基⾦教授(⽣物無機化學)孫紅哲及其研究團隊王素⽟、李洪艷、孫紅哲、王潤銘、袁碩峰和陳福和。




